近日,西北大学生命科学学院李想教授团队在骨髓微环境调控髓系肿瘤免疫逃逸研究中取得重要进展,揭示了一种全新的“糖链调控-免疫塑形”机制。相关研究成果以研究长文(Article)形式发表于国际血液学权威期刊《Haematologica》,题为:“Bisecting GlcNAc expression by bone marrow stromal cells modulates TGF-β1-driven macrophage polarization in myeloid leukemias”。

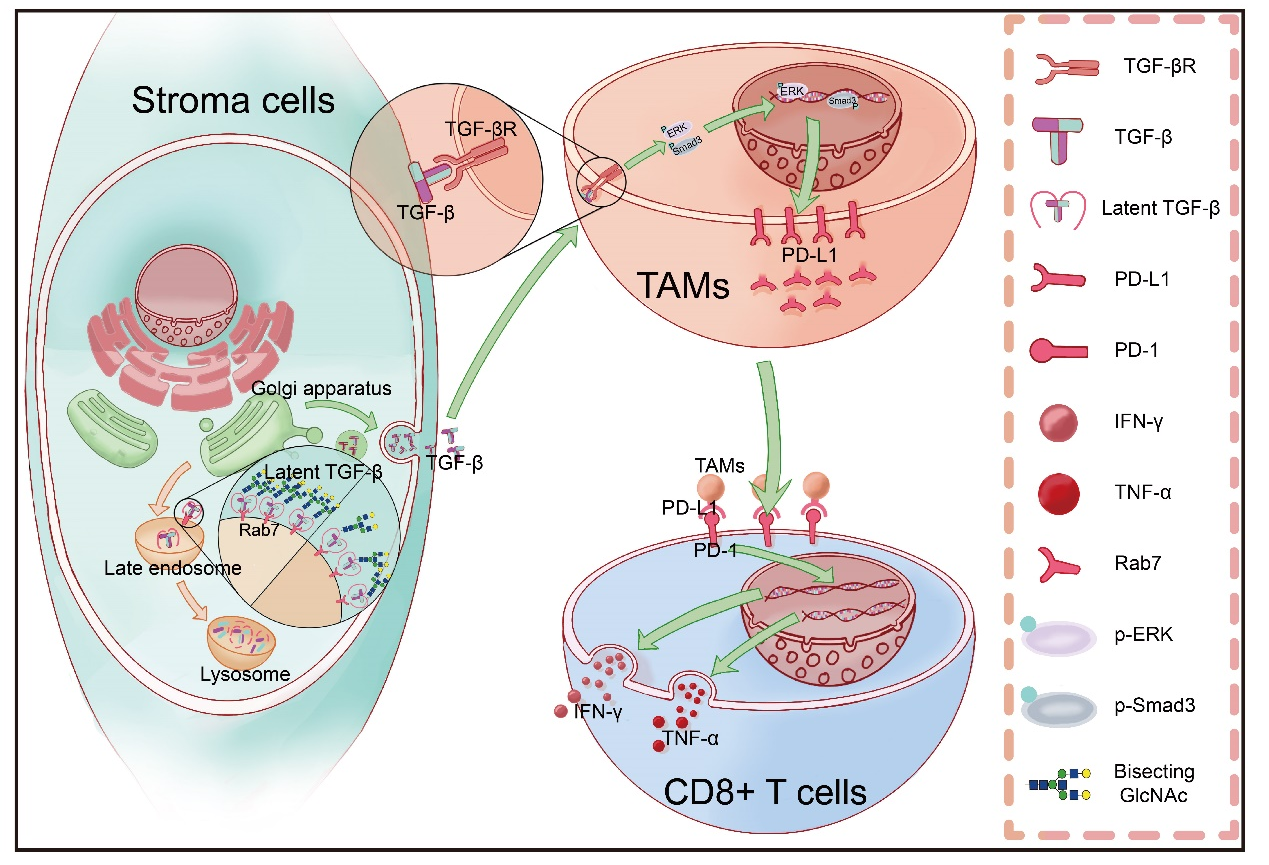
肿瘤相关巨噬细胞(TAMs)在髓系肿瘤免疫逃逸和疾病进展中发挥关键作用。本研究结合单细胞转录组测序、流式细胞术和蛋白质组学技术,系统揭示:MDS/AML患者骨髓基质细胞中平分型N-乙酰葡萄糖胺(bisecting GlcNAc)水平显著下调,导致TGF-β1分泌增加,进而诱导巨噬细胞向M2亚型极化,并上调PD-L1表达,抑制CD8⁺ T细胞功能,从而形成利于恶性克隆细胞存活和扩增的免疫抑制微环境。
肿瘤相关巨噬细胞(TAMs)在髓系肿瘤免疫逃逸和疾病进展中发挥关键作用。本研究结合单细胞转录组测序、流式细胞术和蛋白质组学技术,系统揭示:MDS/AML患者骨髓基质细胞中平分型N-乙酰葡萄糖胺(bisecting GlcNAc)水平显著下调,导致TGF-β1分泌增加,进而诱导巨噬细胞向M2亚型极化,并上调PD-L1表达,抑制CD8⁺ T细胞功能,从而形成利于恶性克隆细胞存活和扩增的免疫抑制微环境。
《Haematologica》为中科院一区TOP期刊,最新影响因子IF=8.2。西北大学2023级博士研究生丰晶晶(现为中法联合培养博士生)、2022级博士研究生勾俊杰与陕西省人民医院血液科王一主任为共同第一作者,李想教授为唯一通讯作者。研究工作获得国家自然科学基金重大培育项目和面上基金、陕西省杰出青年项目和陕西省创新团队项目等资助。这项工作是继团队此前在《Leukemia》《Journal of Extracellular Vesicles》《Redox Biology》《Theranostics》上的连续发表后,在髓系肿瘤微环境机制研究领域的又一重要突破。
全文链接: