近日,西北大学生命科学学院严健教授团队在《International Journal of Biological Sciences》(中科院一区TOP期刊,IF=8.2)发表题为“Unlocking the Puzzle of Mammalian Transfection: The Role of the RNA-sensing-Mediated Interferon Response in the Cellular Defense Against Foreign DNA Intrusion”的研究论文,系统揭示了哺乳动物细胞中限制转染效率的关键分子机制。

将外源DNA导入哺乳动物细胞以驱动目标基因表达,是分子生物学研究和基因治疗应用中的关键技术。尽管现有多种策略可用于提高转染效率,但在多数细胞类型中,尤其是相较于高效易转染的HEK293T细胞,转染效率依然偏低。因此亟需提升转染效率及外源基因表达水平,这在多个研究领域均具有重要意义。
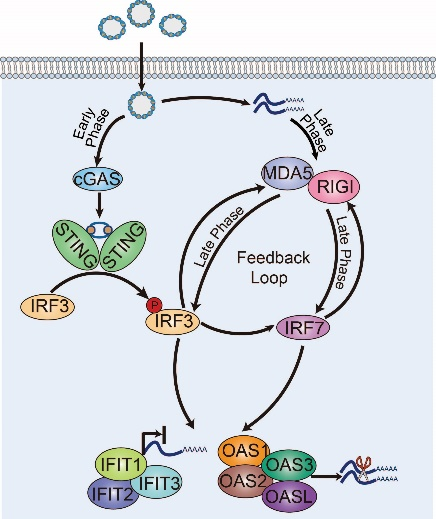
该团队利用RNA-seq与ChIP-seq技术,系统描绘了环状与线性DNA在五种人源细胞中的免疫反应谱系。该研究发现,在cGAS-STING通路以及下游IRF3/7转录因子的调控下,多个RNA处理相关通路,包括RNA感应基因(如MDA5、RIGI),RNA降解相关基因(OAS1/2/3/L)以及翻译抑制相关基因(IFIT1/2/3),共同参与抑制转基因表达。该研究还发现,线性DNA比环状DNA更容易引起细胞的免疫应激,且转染激活的免疫反应通路会在染色质水平产生表观遗传记忆,并在细胞复制时保留,从而在后续再次转染时进一步抑制转染效率。
此外,团队进一步证实,抑制RNA感应通路及cGAS-STING通路可显著提高转基因表达水平,其中STING与MDA5的双重抑制效果最为显著,进一步凸显DNA和RNA感应机制在诱导干扰素刺激基因(ISGs)表达及抑制转基因表达中的协同作用。该研究首次明确RNA感应机制在转染免疫应答中的作用,提出通过阻断cGAS-STING与RNA感应轴,可显著提升外源基因表达,为基因治疗、疫苗开发与细胞工程提供重要理论依据。
西北大学生命科学学院博士生李晓雨和香港城市大学博士生周奕岑为共同第一作者,严健教授为通讯作者。该工作得到国家自然科学基金委、深圳市医学研究基金、香港研究资助局以及陕西省基础科学(化学、生物学)研院等项目的资助支持。
参考文献:
1. Kim TK, Eberwine JH. Mammalian cell transfection: the present and the future. Analytical and bioanalytical chemistry. 2010; 397: 3173-8.
2. Fus-Kujawa A, Prus P, Bajdak-Rusinek K, Teper P, Gawron K, Kowalczuk A, et al. An Overview of Methods and Tools for Transfection of Eukaryotic Cells in vitro. Frontiers in bioengineering and biotechnology. 2021; 9: 701031.
3. Hopfner KP, Hornung V. Molecular mechanisms and cellular functions of cGAS-STING signalling. Nat Rev Mol Cell Biol. 2020; 21: 501-21.
4. Majerciak V, Zheng ZM. Induction of translation-suppressive G3BP1(+) stress granules and interferon-signaling cGAS condensates by transfected plasmid DNA. hLife. 2025; 3: 21-37.
5. Brisse M, Ly H. Comparative Structure and Function Analysis of the RIG-I-Like Receptors: RIG-I and MDA5. Front Immunol. 2019; 10: 1586.
6. Fan L, Sun W, Lyu Y, Ju F, Sun W, Chen J, et al. Chrom-seq identifies RNAs at chromatin marks. Science advances. 2024; 10: eadn1397.